- Détails
- Affichages : 14464
Faut-il avoir peur des spores de champignons ?
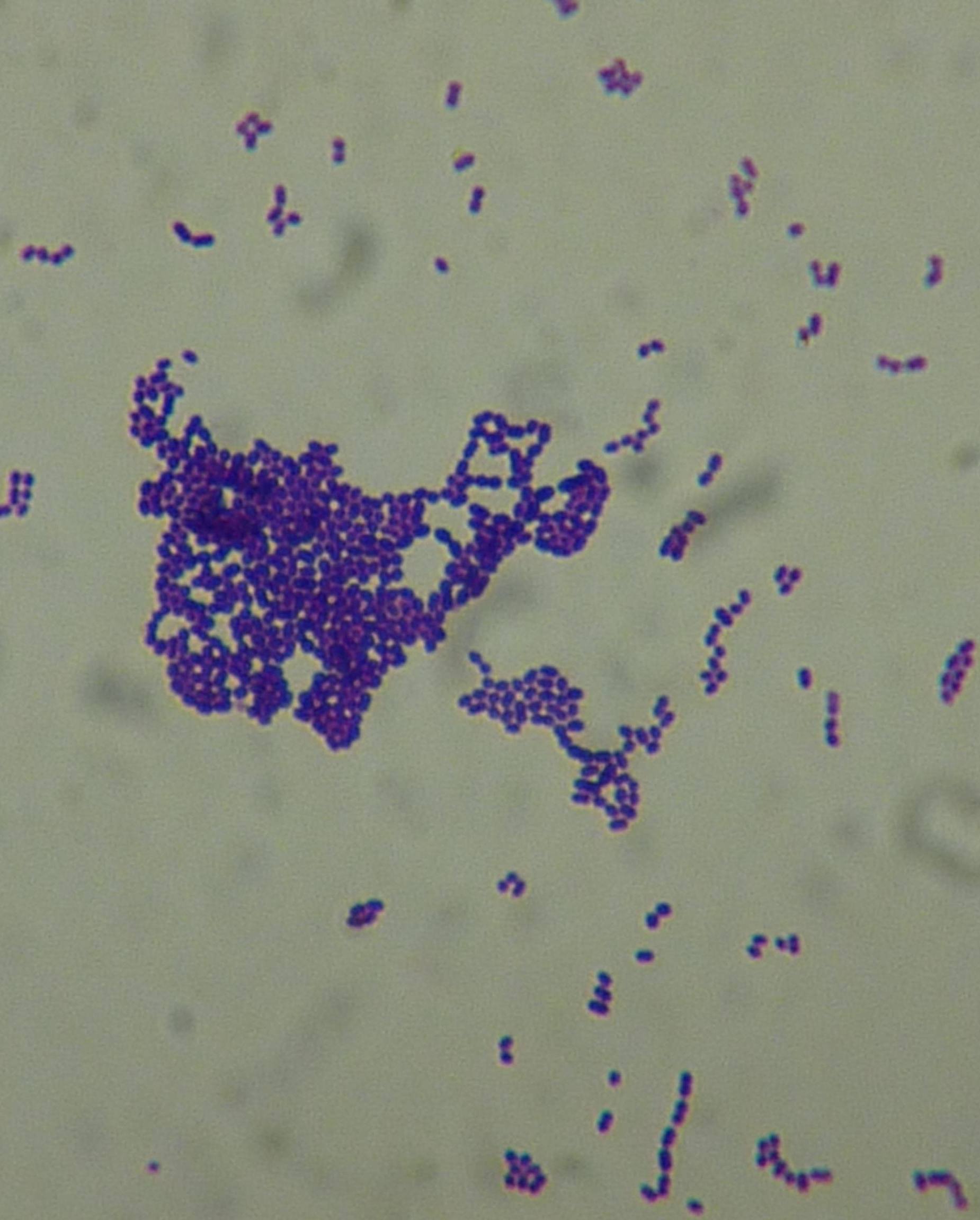
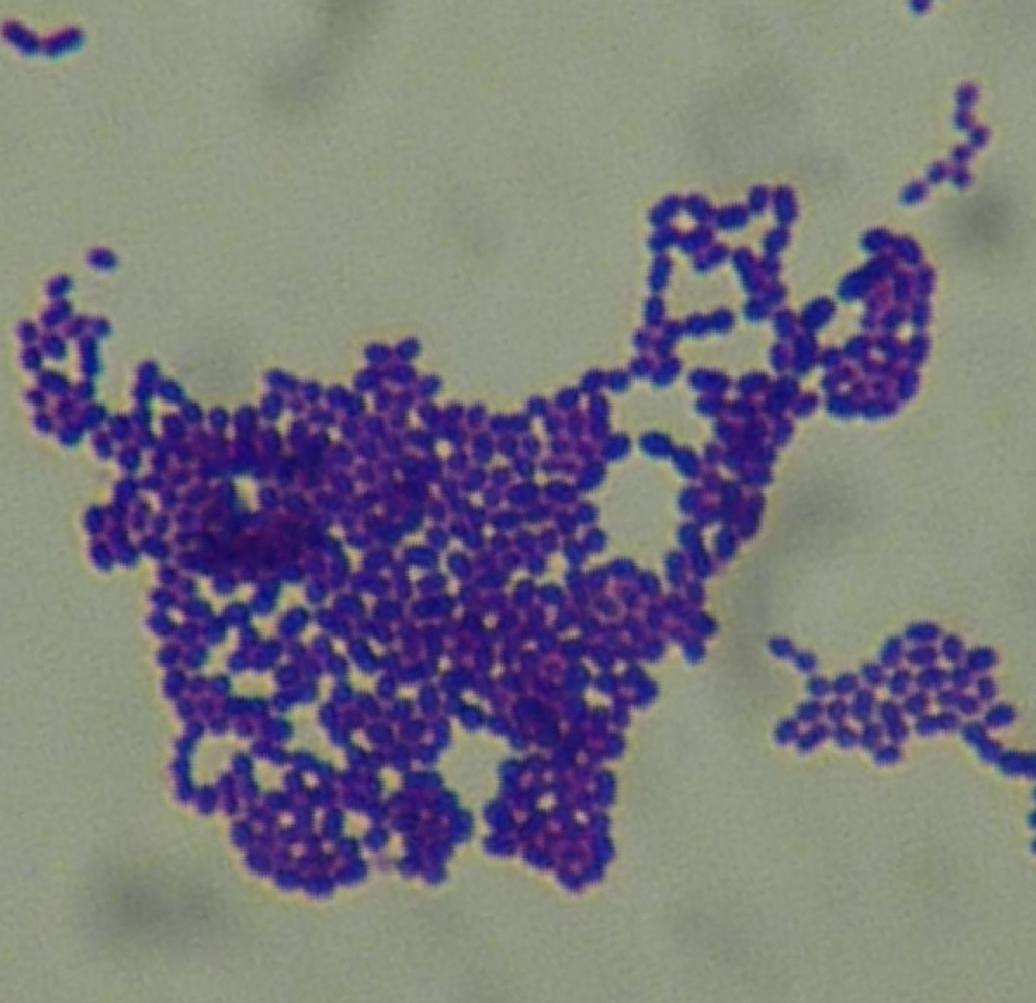
Depuis de nombreuses années, on entend parler des spores d’Aspergillus qui forment des aérosols massifs quand on les manipule au laboratoire et qui provoquent des maladies gravissimes chez les élèves. De toutes parts arrive la recommandation d'utiliser un PSM pour manipuler des moisissures banales comme Aspergillus. C'est le cas aux examens (bac), à l'INRS. Et voilà qu’il faut les manipuler sous PSM avec un scaphandre…
Il me semble pourtant que la première action à faire avant de prendre des mesures contraignantes, coûteuses et stupides est l'analyse de risques.
Première observation :combien de malades dans les laboratoires (d'établissements scolaires) ?
La réponse est très claire : AUCUN (officiellement). Le seul cas suspect rencontré chez un collègue il y a de nombreuses années en Normandie s’avère faux. Regardons les aspergilloses en France : on ne les trouve que dans les services d’immunodéprimés, et tout particulièrement les leucémiques et les greffés de moelle. Peut-être existe-t-il encore quelques cas chez des paysans ayant respiré des quantités massives de spores dans des silos que les moisissures ont envahi. Comment les malades ont-ils été atteints ? Il a fallu que des spores les contaminent : elles proviennent souvent de travaux voisins sur des bâtiments. Constatons que ce sont les seuls atteints car les ouvriers, plus exposés, ne sont pas tombés malades. Nous avons donc une excellente immunité contre les Aspergillus.
Deuxième observation : les contaminations des boîtes de bactériologie ou de culture cellulaire au lycée.
Au lycée Paul Éluard, nous manipulons champignons, cellules et bactéries dans le même laboratoire, nous cultivons les cellules sans antifongiques, et bien évidemment le labo est occupé au moins 30 à 40 h par semaine… Et pourtant les contaminations fongiques sont rares…
Ajoutons même que nous avons isolé un A. fumigatus du bac à eau de l’étuve à CO2 alors que nous ne l’avions pas dans le souchier… donc qu’il provenait de l’environnement et qu’il fallait mettre un antifongique dans le bac à eau (ou renouveler souvent cette eau) (voir Champignons dans étuve à CO2). De plus, des champignons comme les Aspergillus cultivent très rapidement (en 24 h) et à 37°C…
Enfin, une technicienne de mycologie à l'hôpital Avicenne (Bobigny) m'a gentiment fait remarquer que les champignons des différents tubes placés dans l'étuve ne passent pas de tubes en tubes !
Troisième observation :
quand on fait du camembert, les ouvriers pulvérisent Penicillium camembertii sous forme d’aérosol, sans masque ni autre protection (au moins dans la laiterie visitée)… Bien sûr cette moisissure n'est pas pathogène…
Quatrième observation :
les champignons ne sautent pas d’un tube à l’autre dans le souchier tenu normalement. Il est facile de le constater en regardant les tubes…
Il me semble donc qu'imposer la manipulation sous PSM des moisissures n'est pas sérieux car, si le danger existe, il n'y a pas de réel risque puisque l'aérolisation est très limitée, que les apprenants ne sont pas dans les catégories à risque. De plus, les PSM ayant aussi pour fonction la culture cellulaire, il est dommage de les contaminer avec des spores d'Aspergillus.
Je répète donc qu'il nous faut, avant toute décision contraignante, analyser pour déterminer les meilleures mesures à prendre pour limiter le risque. On ne peut évidemment pas oublier la règlementation ni la situation professionnelle dans les laboratoires concernés, c'est-à-dire les LBM essentiellement, dans lesquels la règlementation n'est quasiment JAMAIS appliquée. On ne peut pas imposer un P4 pour la manipulation des microorganismes depuis la classe 2 (et pourquoi pas 1). L'absence de réflexion ne peut que conduire à des dérives regrettables soit le laxisme (en particulier dans les LBM) soit d'excès de précaution.
Enfin, on ne peut imposer que si l'on fait l'effort de répondre à des arguments par des arguments sérieux et non par un simple diktat.
Bine sûr, la manipulation des champignons, comme celle des autres agents biologiques, mérite toutes les précautions nécessaires pour éviter la contamination des élèves et de l’environnement. Les bonnes pratiques normales du laboratoire suffisent largement à cet objectif. Le risque biologique lié aux champignons est extrêmement limité tant qu’on ne manipule pas Histoplasma ou Blastomyces ! (classe 3)
PS1 : la recherche sur internet de statistiques sur les aspergillose a été vaine. Un article sur sante.gouv.fr parle de 621 cas dans 18 hopitaux parisiens en 5 ans (soit 100 cas par an) uniquement chez des patients à risque (neutropénie (y compris leucémies ?), corticothérapie long cours, greffes de moelle, aspergillose antérieures…) avec un taux de mortalité très élevé.
PS2 : pour les BTS Analyses de biologie médicale (et DUT correspondant), l’utilisation des dermatophytes est obligatoire. Les souches proviennent forcément de laboratoires et sont pathogènes… Mesurons le taux de teignes et autres épidermophyties pour évaluer le risque !