On peut clairement dire qu'une galerie traditionnelle n'est pas réellement une solution pour identifier ces bactéries. On peut touefois faire un peu comme pour les Entérobactéries... Voici une galerie possible :
| Milieu | Test à réaliser |
Résultats lisibles |
| Gélose ordinaire ou autre milieu équivalent |
Examens microscopiques Oxydase |
Pureté, macroscopie, production de pigments, culture, Gram, Mobilité et son type |
| VF (remplaçable par la lecture du culot de Kligler) |
Type respiratoire | |
| Hugh et Leifson glucosé | Voie d'attaque du Glucose | |
|
Kligler (glucose-lactose-H2S) |
recherche éventuelle de l'ONPG hydrolase |
Fermentation ou non du glucose et Gaz en glucose |
| Mannitol-Mobilité-Nitrates | recherche des nitrites | Utilisation du mannitol Production de gaz (qui peut être du diazote si man -) Culture en profondeur par respiration nitrates si la souche est aérobie stricte |
| Urée Tryptophane |
TDA, Indole | Uréase Tryptophanase (Indole) Tryptophane désaminase (TDA) |
| Citrate de Simmons |
Utilisation du Citrate comme seule source de Carbone | |
| Clark et Lubs (bouillon riche glucosé) |
VP et pour les nostalgiques RM (si 48 h) |
Production de 3-hydroxybutanone et dérivés |
| ADH, LDC, ODC |
ADH, LDC, ODC (attention : pour les aérobies strictes il n'y aura pas de culture... sauf pour ADH parfois. La lecture n'est donc pas possible le plus souvent sauf pour une ADH+. Mieux vaut ensemencer une API20E ! | |
| Film photographique… | Gélatinase | |
|
(O129 (disque sur la GO)) |
S/R au composé O129 si soupçon de Vibrio/aeromonas |
La galerie traditionnelle peut être remplacée par un équivalent réalisé en microplaque.
Cette galerie traditionnelle sera évidemment remplacée avantageusement par une microgalerie commercialisée.
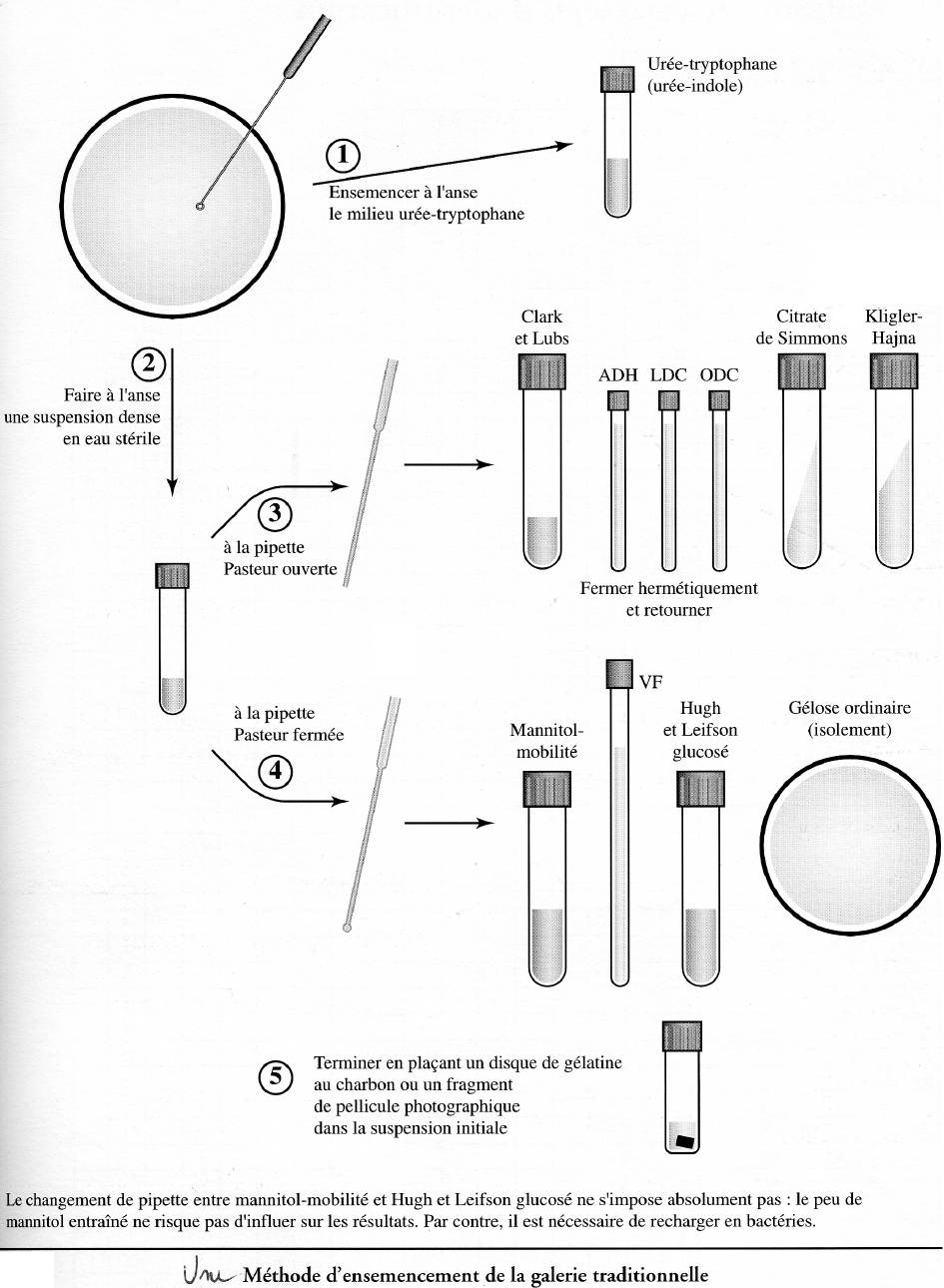
Ensemencement (extrait de Documentation technique)
La technique décrite ici repose sur une optimisation destinée à réduire au maximum le matériel utilisé et le temps ! On peut estimer, une fois les milieux préparés, un ensemencement réalisé en quelques minutes.
- L'anse est utilisée pour préparer la suspension.
- La pipette ouverte (qui permet la rapidité) pour le maximum de milieux.
- La pipette fermée sert à réaliser les milieux piqués et l'isolement. Il ne faut pas craindre le passage d'un peu de milieu d'un milieu au suivant. En commençaut par Mannitol mobilité, on s'évite une éventuelle pollution par le glucose.
shock drop air force 1 full uv reactive | Sb-roscoffShops - An Ode to The Air Jordan 11: The Greatest Hoop Sneaker of the 90s - nike zoom kobe vi hollywood 3d printing machine

